иҝ‘ж—Ҙ�������пјҢзҺҜеҢ–еӯҰйҷўиҖҝејјжұҹеүҜй’»з ”е‘ҳеңЁNatureеӯҗеҲҠгҖҠNature CommunicationsгҖӢдёҠйўҒеҸ‘йўҳдёәвҖңD-ПҖ-A sensitized carbon dots as long-lived type-I/II photosensitizers for NIR-excited hypoxia-regulated photodynamic therapyвҖқзҡ„й’»з ”и®әж–Ү����гҖӮ
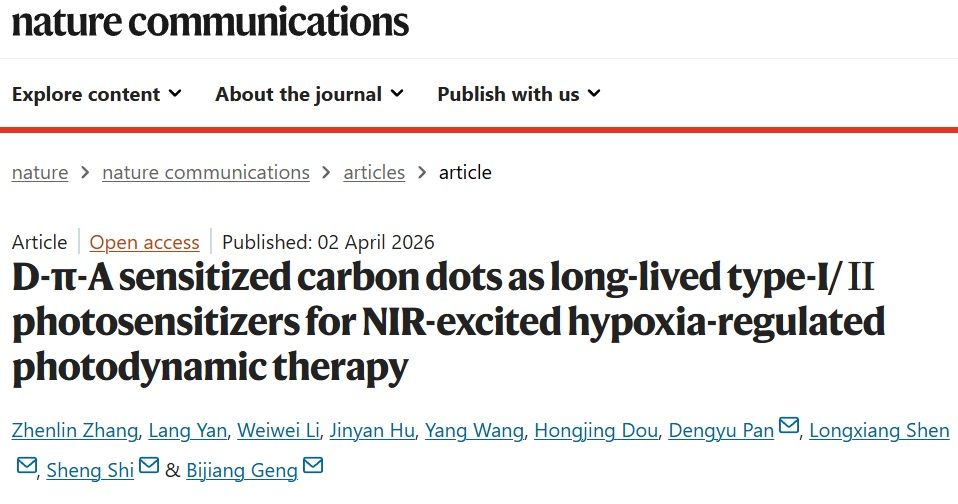
е…үеҠЁеҠӣеҢ»жІ»пјҲPDTпјүеҮӯеҖҹе…¶йқһдҫөе…ҘжҖ§гҖҒж—¶з©әеҸҜжҺ§е’Ңе…Қз–«жҝҖжҙ»и№¬зқҖеҠҝ�������пјҢеңЁиӮҝзҳӨеҢ»жІ»йўҶеҹҹеұ•зӨәеҮәе·ЁеӨ§жҪңеҠӣ����гҖӮ然иҖҢ�������пјҢдј з»ҹе…үж•ҸеүӮжҷ®йҒҚйқўеҜ№еј•еҸ‘жіўй•ҝзҹӯгҖҒдёүжІүжҖҒеҜҝе‘ҪзҹӯгҖҒдҫқиө–ж°§ж°”дә§з”ҹеҚ•зәҝжҖҒж°§зӯү瓶йўҲ�������пјҢеҜјиҮҙе…¶еңЁд№Ҹж°§иӮҝзҳӨеҫ®зҺҜеўғдёӯзҡ„з–—ж•ҲдёҘжІүеҸ—йҷҗ����гҖӮжӯӨиЎЁ�������пјҢиӢҘдҪ•е®һзҺ°еҚ•дёҖиҝ‘зәўиЎЁжҝҖе…үеј•еҸ‘дёӢзҡ„I/IIеһӢеҸҢжЁЎејҸPDTдёҺе’Ңе–„е…үзғӯеҢ»жІ»пјҲPTTпјүзҡ„еҚҸеҗҢ�������пјҢеҗҢж—¶йў„йҳІеҜ№жӯЈеёёз»„з»Үзҡ„зғӯеҚұйҷ©�������пјҢжҳҜеҪ“еүҚPDTйўҶеҹҹдәҹеҫ…и§ЈеҶізҡ„关键科еӯҰй—®йўҳ����гҖӮ
й’ҲеҜ№дёҠиҝ°жҢ‘жҲҳ�������пјҢжҪҳзҷ»дҪҷ/иҖҝејјжұҹй’»з ”еӣўйҳҹеҸ‘еұ•дәҶдёҖз§ҚдәҢе…ғеүҚдҪ“е·ҘзЁӢжҲҳжңҜ�������пјҢйҖҡиҝҮзІҫеҮҶи°ғжҺ§зўізӮ№зҡ„з»ҷдҪ“-ПҖ-еҸ—дҪ“пјҲD-ПҖ-Aпјүжһ„еһӢ�������пјҢд»Ҙй…ҡзҫҹеҹәдёәеҜҢз”өеӯҗз»ҷдҪ“гҖҒеҗЎе•¶ж°®дёәеҗёз”өеӯҗеҸ—дҪ“�������пјҢжһ„зӯ‘дәҶжӢҘжңүи¶…й•ҝдёүжІүжҖҒеҜҝе‘ҪпјҲ36.2 msпјүзҡ„иҝ‘зәўиЎЁе“Қеә”еһӢI/IIеҸҢжЁЎејҸе…үж•ҸеүӮпјҲP-CDsпјү����гҖӮзҗҶи®әжҺЁз®—дёҺе°қиҜ•дәҶеұҖжү№жіЁ�������пјҢD-ПҖ-Aз»“жһ„иҜұеҜјзҡ„еҲҶеӯҗеҶ…з”өиҚ·иҪ¬з§»жҖҒжһҒеӨ§жҺЁиҝӣдәҶзі»й—ҙзӘңи¶Ҡ�������пјҢзј©е№јдәҶеҚ•жІүжҖҒ-дёүжІүжҖҒиғҪйҡҷ�������пјҢд»ҺиҖҢе®һзҺ°дәҶй«ҳж•Ҳзҡ„еҚ•зәҝжҖҒж°§пјҲ1O2пјүе’Ңи¶…ж°§йҳҙзҰ»еӯҗиҮӘз”ұеҹәпјҲO2?ЛүпјүеӨ©з”ҹ����гҖӮдёҺжӯӨеҗҢж—¶�������пјҢP-CDsйҳҗеҸ‘еҮәе’Ңе–„зҡ„е…үзғӯиҪ¬жҚўж•ҲиғҪпјҲ32.2%пјү�������пјҢеҸҜеңЁдҪҺеҠҹзҺҮеҜҶеәҰпјҲ0.30 W/cm2�������пјҢ808 nmпјүдёӢе®һзҺ°е’Ңе–„зҡ„е…үзғӯеҢ»жІ»�������пјҢжңүж•Ҳзј“и§ЈиӮҝзҳӨд№Ҹж°§�������пјҢиҝӣдёҖжӯҘеҠ ејәPDTз–—ж•Ҳ����гҖӮй’»з ”еӣўйҳҹиҝӣдёҖжӯҘйҖүеҸ–M1еһӢе·Ёеҷ¬з»ҶиғһиҶңе°ҒиЈ…P-CDsпјҲP-CD@MMпјү�������пјҢе®һзҺ°дәҶиҮӘеҠЁйқ¶еҗ‘иӮҝзҳӨеҜҢйӣҶдёҺжҖҘеү§зі»з»ҹжҖ§ж–ӯж №����гҖӮеңЁеҸҢдҫ§иҚ·зҳӨе№јйј жЁЎеһӢдёӯ�������пјҢз»ҸиҝҮйқҷи„үжіЁе°„з»“еҗҲеҚ•ж¬Ўиҝ‘зәўиЎЁжҝҖе…үз…§е°„�������пјҢжңүж•ҲжҠ‘йҖ дәҶеҺҹеҸ‘иӮҝзҳӨзҡ„жҲҗй•ҝ�������пјҢиҝҳйҖҡиҝҮиҜұеҜје…Қз–«еҺҹжҖ§ж®’е‘ҪгҖҒжҺЁиҝӣж ‘зӘҒз»ҶиғһжҲҗзҶҹгҖҒе°ҶиӮҝзҳӨжңүе…іе·Ёеҷ¬з»Ҷиғһд»ҺдҝғиӮҝзҳӨзҡ„M2иЎЁеһӢжІүжһҒеҢ–дёәжҠ—иӮҝзҳӨзҡ„M1иЎЁеһӢ�������пјҢжҳҫи‘—жҠ‘йҖ дәҶиҝңз«ҜиӮҝзҳӨзҡ„жҲҗй•ҝ�������пјҢ并жҲҗз«ӢдәҶжҢҒд№…е…Қз–«еҪұиұЎж•Ҳеә”����гҖӮ
зҺҜеҢ–еӯҰйҷў24зә§еҚҡеЈ«й’»з ”з”ҹеј й•Үжһ—дёәжң¬ж–Ү第дёҖдҪңиҖ…�������пјҢиҖҝејјжұҹеүҜй’»з ”е‘ҳгҖҒжҪҳзҷ»дҪҷй’»з ”е‘ҳгҖҒдёҠжө·дәӨйҖҡеӨ§еӯҰеҢ»еӯҰйҷўд»Һеұһ第е…ӯдәәж°‘еҢ»йҷўжІҲйҫҷзҘҘж•ҷжҺҲ�������пјҢеҗҢжөҺеӨ§еӯҰд»Һеұһ第еҚҒдәәж°‘еҢ»йҷўеҸІеҚҮеүҜж•ҷжҺҲдёәе…ұеҗҢйҖҡи®ҜдҪңиҖ…����гҖӮдәҝдёҮе…Ҳз”ҹMRдёә第дёҖе®һзҺ°еҚ•е…ғе’ҢйҖҡи®ҜеҚ•е…ғ����гҖӮиҜҘй’»з ”еҫ—еҲ°дәҶеӣҪеәҰеӨ©з„¶з§‘еӯҰеҹәйҮ‘гҖҒдёҠжө·еёӮеӨ©з„¶з§‘еӯҰеҹәйҮ‘гҖҒдёӯеӣҪ科еҚҸйқ’е№ҙдәәжүҚжүҳдёҫе·ҘзЁӢзӯүйЎ№дё»еј иөһеҠ©����гҖӮ
и®әж–Үй“ҫжҺҘпјҡhttps://doi.org/10.1038/s41467-026-71476-y








