еҹәдәҺж— жңәзәізұійў—зІ’гҖҒзәізұіи„ӮиҙЁдҪ“зӯүзәізұізІ’еӯҗзҡ„иҚҜзү©йҖ’йҖҒзі»з»ҹ������пјҢжӢҘжңүеңЁжҙ»дҪ“еҶ…йқ¶еҗ‘йҖ’йҖҒиҜҠз–—иҜ•еүӮзҡ„жҪңеҠӣ������пјҢиҝ‘е№ҙжқҘеңЁзҷҢз—ҮеҢ»жІ»е’Ңз–«иӢ—ејҖеҸ‘дёӯеҸ—еҲ°дәҶе®Ҫжіӣе…іжіЁ��������гҖӮ然иҖҢ������пјҢеӨ§йғЁй—ЁзәізұізІ’еӯҗеңЁиҝӣе…ҘиЎҖж¶ІеҫӘзҺҜеҗҺдјҡиў«иӮқи„Ҹе·Ёеҷ¬з»ҶиғһпјҲеҰӮKupfferз»ҶиғһпјүжҚ•иҺ·������пјҢеҜјиҮҙиҚҜзү©ж— жі•жңүж•ҲиҫҫеҲ°иӮҝзҳӨйғЁдҪҚ��������гҖӮиҝҷжҲҗдёәдәҶзәізұізІ’еӯҗйқ¶еҗ‘йҖ’йҖҒжҠҖжңҜзҡ„дёҖдёӘйҮҚиҰҒжҢ‘жҲҳ��������гҖӮиҝҷз§ҚжҷҜиұЎйҖҡеёёжҳҜз”ұдәҺзәізұізІ’еӯҗиЎЁиЎЁеҗёйҷ„иЎҖжё…иӣӢзҷҪиҙЁпјҲеҪўжҲҗвҖңиӣӢзҷҪиҙЁеҶ вҖқпјүжүҖиҮҙ������пјҢиҜҘиҝҮзЁӢдјҡи§ҰеҸ‘иӮқи„Ҹдёӯзҡ„еҗһеҷ¬дҪңз”Ё������пјҢжҳҫи‘—йҷҚдҪҺдәҶзәізұізІ’еӯҗзҡ„иҫҫеҲ°йқ¶зӮ№зҡ„жҰӮзҺҮ������пјҢ并еўһй•ҝдәҶиӮқи„ҸзҙҜз§ҜжҜ’жҖ§��������гҖӮеӣ иҖҢ������пјҢиӢҘдҪ•иәІйҒҝиӮқи„ҸжҚ•иҺ·е№¶жҸҗй«ҳиӮҝзҳӨйқ¶еҗ‘йҖ’йҖҒж•ҲиғҪдёҖеҗ‘жҳҜзәізұіеҢ»еӯҰйўҶеҹҹзҡ„дёҖдёӘжІүеӨ§жҢ‘жҲҳ��������гҖӮ
иҝ‘жңҹ������пјҢдәҝдёҮе…Ҳз”ҹMRзҗҶеӯҰйҷўиҜёйў–й’»з ”е‘ҳгҖҒзҺӢдёҪеҚҺй’»з ”е‘ҳдёҺдёҠжө·дәӨйҖҡеӨ§еӯҰжЁҠжҳҘжө·ж•ҷжҺҲеҗҲдҪң������пјҢејҖеҸ‘дәҶдёҖз§ҚеҗҚдёәвҖңйҡҗеҪўеӨ§ж°…вҖқзҡ„зәізұізІ’еӯҗиЎЁиЎЁе·ҘзЁӢжҠҖжңҜ������пјҢжҲҗеҠҹе®һзҺ°дәҶзәізұізІ’еӯҗеңЁдҪ“еҶ…зҡ„й«ҳж•ҲиӮҝзҳӨйқ¶еҗ‘йҖ’йҖҒ��������гҖӮиҝҷйЎ№й’»з ”зҡ„дё»йўҳжҳҜеҲ©з”ЁDNAеҲҶеӯҗеұӮдҪңдёәзәізұізІ’еӯҗзҡ„еҸҜйҷҚи§Јж¶ӮеұӮ��������гҖӮиҝҷдёҖеұӮDNAдёҚд»…иғҪеҗёйҷ„иЎҖжё…дёӯзҡ„жҠ—еҗһеҷ¬иӣӢзҷҪпјҲеҰӮеҜҢеҗ«з»„ж°Ёй…ёзҡ„зі–иӣӢзҷҪпјү������пјҢд»ҺиҖҢеңЁиӮқи„ҸдёӯжҸҗдҫӣиҒҢиғҪжҖ§зҡ„вҖңйҡҗеҪўвҖқжҲҗж•Ҳ������пјҢиҝҳиғҪеңЁиӮҝзҳӨзҺҜеўғдёӯйҖҡиҝҮDNAйҷҚи§ЈжқҘи§ҰеҸ‘иӮҝзҳӨзү№ејӮжҖ§ж‘„еҸ–������пјҢжңүе…іжҲҗе°ұеңЁгҖҠJournal of the American Chemical SocietyгҖӢдёҠйўҒеҸ‘��������гҖӮ
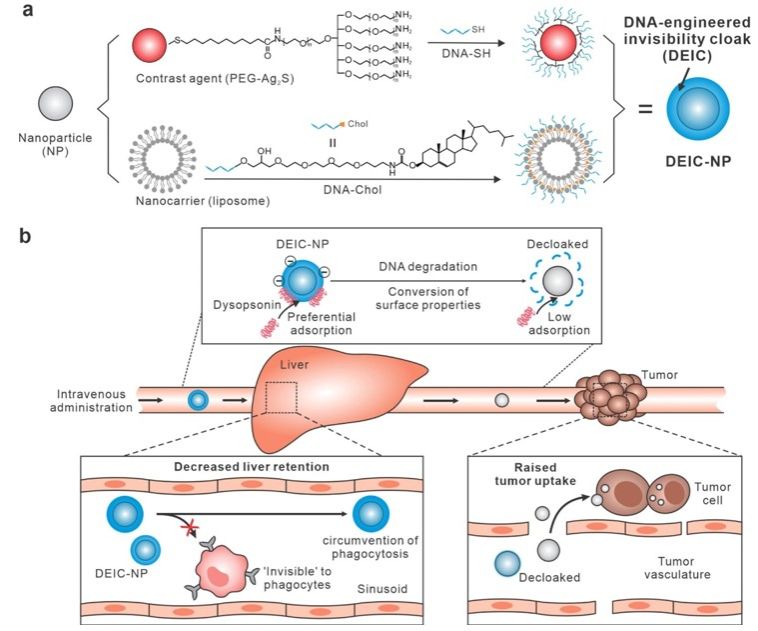
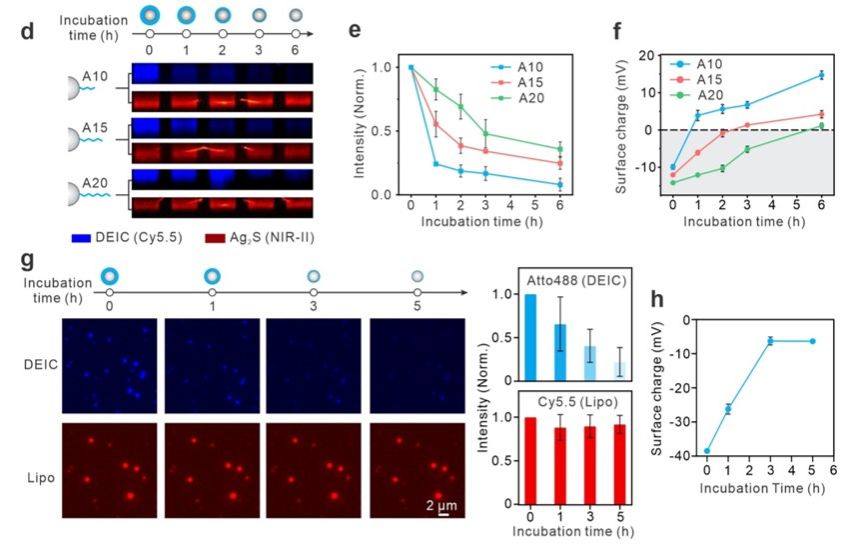
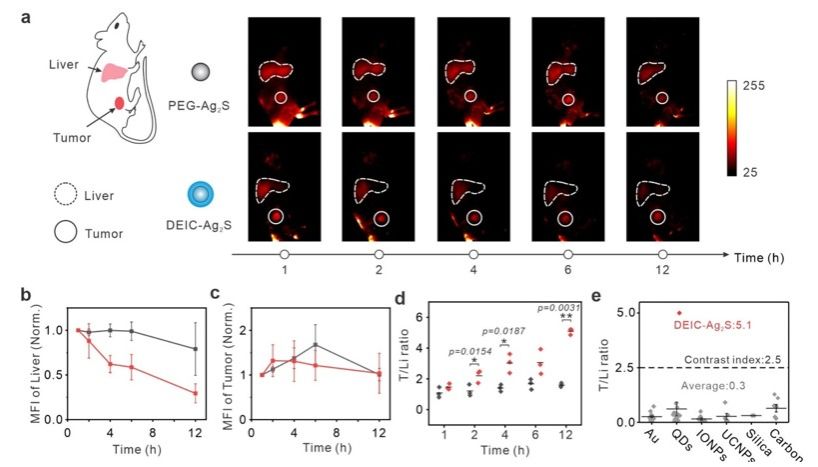
еңЁй’»з ”дёӯ������пјҢеӣўйҳҹйҖүжӢ©дәҶзЎ«еҢ–银йҮҸеӯҗзӮ№е’Ңи„ӮиҙЁдҪ“дҪңдёәжЁЎеһӢзәізұізІ’еӯҗ������пјҢдҪҝз”ЁDNAеҲҶеӯҗиҝӣиЎҢдәҶеҜҶйӣҶеҢ…иҰҶ������пјҢеҪўжҲҗдәҶеҸҜйҷҚи§ЈйҡҗеҪўеӨ§ж°…зәізұізІ’еӯҗ��������гҖӮ并且������пјҢиҝҷз§ҚйҡҗеҪўеӨ§ж°…зҡ„йҷҚи§ЈйҖҹеәҰиғҪеӨҹйҖҡиҝҮDNAй“ҫзҡ„й•ҝеәҰиҝӣиЎҢеҸҜзј–зЁӢзҡ„и°ғжҺ§��������гҖӮдҫӢеҰӮ������пјҢиҫғзҹӯзҡ„DNAй“ҫпјҲеҰӮA10пјүжҜ”еҠӣй•ҝзҡ„й“ҫпјҲеҰӮA20пјүйҷҚи§Јеҫ—жӣҙеҝ«������пјҢеӣ иҖҢжӣҙеҝ«ең°и§ҰеҸ‘дәҶзәізұізІ’еӯҗиЎЁиЎЁз”өиҚ·зҡ„иҪ¬еҸҳ������пјҢд»ҺиҖҢеңЁиӮҝзҳӨйғЁдҪҚе®һзҺ°жӣҙй«ҳзҡ„ж‘„еҸ–ж•ҲиғҪ��������гҖӮиҝҷз§ҚеҸҜзј–зЁӢзҡ„йҷҚи§ЈдёӘжҖ§дҪҝеҫ—йҡҗеҪўеӨ§ж°…зәізұізІ’еӯҗзі»з»ҹиғҪеӨҹйҖӮеә”еҲҶжӯ§зҡ„з”ҹзү©зҺҜеўғйңҖиҰҒ������пјҢжҸҗдҫӣдәҶй«ҳеәҰзҹ«жҚ·зҡ„еҲ©з”ЁиҝңжҷҜ��������гҖӮ
еңЁдҪ“еҶ…е№јйј е°қиҜ•дёӯ������пјҢйҖҡиҝҮиҝ‘зәўиЎЁIIеҢәжҲҗеғҸ������пјҢй’»з ”дәәе‘ҳеҸ‘зҺ°йҡҗеҪўеӨ§ж°…еҢ…иЈ№зҡ„зЎ«еҢ–银йҮҸеӯҗзӮ№еңЁиӮҝзҳӨйғЁдҪҚзҡ„е ҶйӣҶйҮҸдёҺиӮқи„ҸзӣёжҜ”������пјҢиҫҫеҲ°дәҶзәҰ5.1зҡ„иӮҝзҳӨ-иӮқи„ҸдҝЎеҸ·жҜ”������пјҢиҝҷдёҖдәҶеұҖжҜ”дј з»ҹзҡ„зәізұіиө„ж–ҷжҸҗй«ҳдәҶзәҰ18еҖҚ��������гҖӮйҷӨдәҶзЎ«еҢ–银йҮҸеӯҗзӮ№д№ӢиЎЁ������пјҢDNAйҡҗеҪўеӨ§ж°…еҢ…иЈ№зҡ„и„ӮиҙЁдҪ“д№ҹе®һзҺ°дәҶиӮҝзҳӨ-иӮқи„ҸдҝЎеҸ·жҜ”зҡ„жҸҗеҚҮ������пјҢжү№жіЁиҝҷз§ҚйҡҗеҪўеӨ§ж°…еҸҜжңӣеҲ©з”ЁдәҺеҲҶжӯ§з§Қзұ»зҡ„зәізұізІ’еӯҗйҖ’йҖҒзі»з»ҹ��������гҖӮжҖ»д№Ӣ������пјҢиҝҷз§ҚеҹәдәҺDNAзҡ„йҡҗеҪўеӨ§ж°…зі»з»ҹдёәиӮҝзҳӨеҢ»жІ»е’ҢзІҫеҮҶеҢ»з–—жҸҗдҫӣдәҶдёҖз§ҚйҖҡз”ЁиҖҢжңүж•Ҳзҡ„е·Ҙе…·������пјҢжңүжңӣеңЁе°ҶжқҘзҡ„зҷҢз—ҮеҢ»жІ»дёӯйҳҗжү¬жІүиҰҒдҪңз”Ё��������гҖӮ
дёҠиҝ°й’»з ”еҫ—еҲ°еӣҪеәҰжІүзӮ№з ”еҸ‘жү“з®—������пјҢеӣҪеәҰеӨ©з„¶з§‘еӯҰеҹәйҮ‘������пјҢдёҠжө·еёӮ2022е№ҙеәҰ"科жҠҖеҲӣж–°иЎҢеҠЁжү“з®—"еҹәзЎҖй’»з ”йўҶеҹҹйЎ№зӣ®е’Ңж–°еҹәзҹій’»з ”е‘ҳйЎ№дё»еј иөһеҠ©��������гҖӮ
и®әж–Үй“ҫжҺҘпјҡhttps://pubs.acs.org/doi/10.1021/jacs.4c09479








